
胶质母细胞瘤(GBM)是成人最常见和最致命的原发性恶性脑肿瘤,在过去的20年里,尽管出现了许多新的治疗方法,但除了标准疗法(手术、放疗和替莫唑胺)之外,胶质母细胞瘤的临床治疗计划仍然不可用。目前,替莫唑胺(TMZ)是延长GBM患者总生存期的化疗药物,因其烷基化DNA的能力而被报道为传统疗法的基石。但是,由于其高度异质性和易突变性,它也是肿瘤耐药性和复发的关键因素。因此,迫切需要确定克服TMZ阻力和提高其治疗效果的更好方法。
近期,天津市环湖医院闫华教授-佟小光教授-徐立霞副研究员团队在Cancer Letters(IF 9.7)期刊上发表了题为“Ultrasound-excited temozolomide sonosensitization induces necroptosis”的文章。该研究首次发现TMZ在超声(US)的影响下会产生活性氧(ROS)。这一特性使得TMZ-US疗法在GBM治疗中具有更好的疗效。鉴于US在中枢神经系统(CNS)疾病中的使用日益增多,以及TMZ对GBM治疗的重要性,有助于TMZ对相关胶质母细胞瘤治疗的发展。中科新生命为该研究提供了4D Labelfree蛋白质组学技术服务。

研究材料
替莫唑胺(TMZ)、人胶质母细胞瘤(GBM)细胞
技术路线
步骤1:TMZ-US在体外增强TMZ对胶质瘤的化疗敏感性;
步骤2:TMZ-US在体内增强抗肿瘤作用;
步骤3:差异甲基化基因和差异表达基因的综合分析;
步骤4:TMZ-US通过增加ROS诱导胶质瘤细胞的坏死凋亡;
步骤5:TMZ-US不能诱导线粒体依赖性细胞凋亡。
研究结果
1. TMZ-US在体外增强TMZ对胶质瘤的化疗敏感性
在本研究中,作者采用不同浓度的TMZ联合相同超声处理TBD、LN229、U87、U251、TMZ耐药的U87/R和U251/R细胞。然后比较IC50值以确定联合治疗的致敏效果。CCK-8结果提示TMZ-US显著增加了胶质瘤细胞的抑制率,并显著降低了TMZ的IC50。同时,作者还检测了细胞凋亡或坏死率和入侵能力,并观察到TMZ-US组显示出比US和TMZ组更高的细胞凋亡或坏死率,侵袭能力更低。ATP浓度的测定也获得了类似的结果。研究表明,ROS在肿瘤细胞中的积累会导致生物分子的氧化,破坏脂质膜和蛋白质的完整性。因此,我们检查了C11-BODIPY581/591的含量并在TMZ-US组中观察到膜脂质过氧化的显著增加。这些结果表明,TMZ-US破坏了线粒体膜电位,导致膜脂质过氧化,细胞功能受损(图1)。
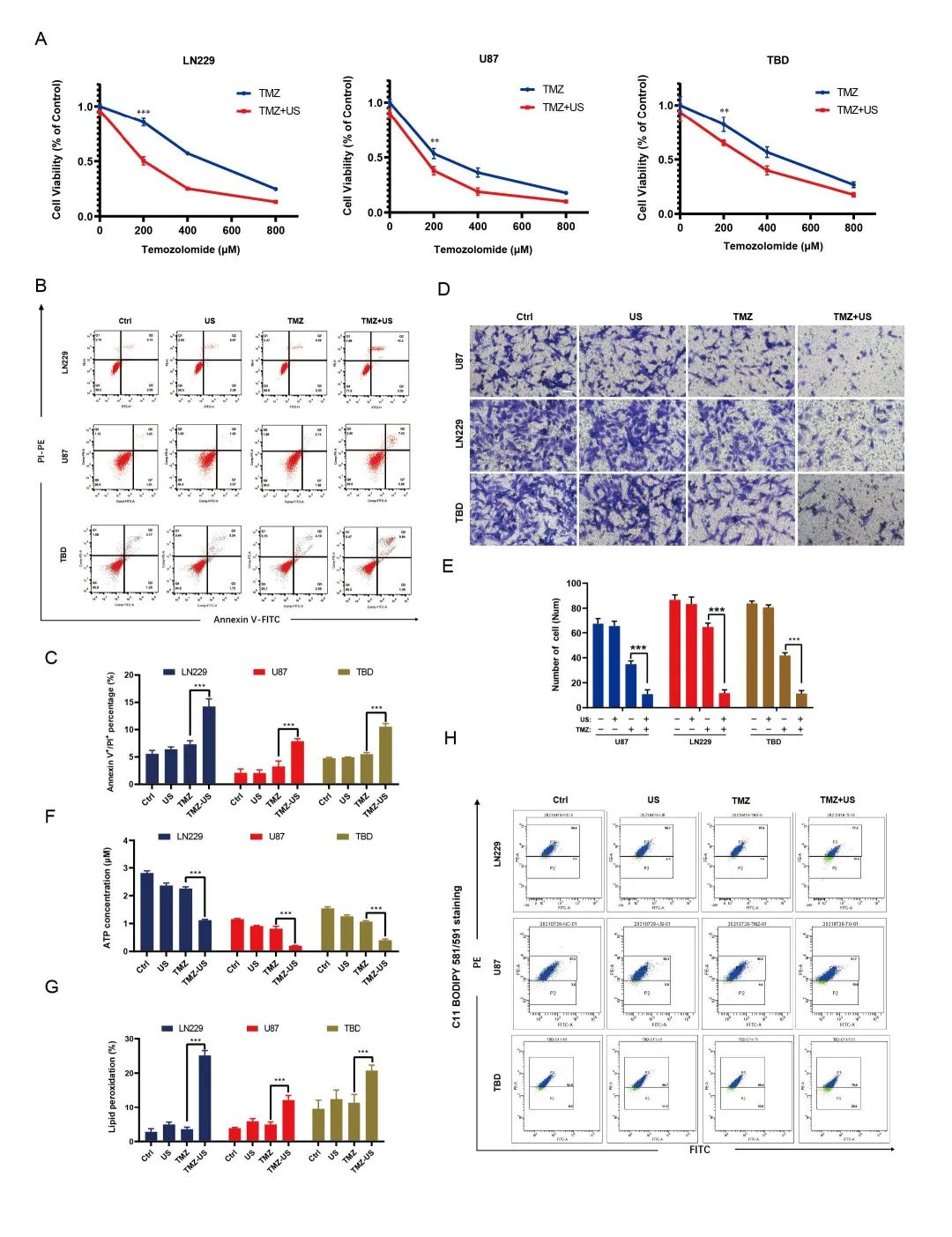
图1 TMZ+US增强TMZ的化疗敏感性
2.TMZ-US在体内增强抗肿瘤作用
作者随后评估联合治疗对皮下肿瘤和神经胶质瘤的抑制作用,与TMZ组相比,使用TMZ-US治疗皮下肿瘤时,观察到肿瘤生长受到显著的抑制。当治疗患有颅内胶质瘤的小鼠时,TMZ-US联合治疗组的体内改善结果显示出比TMZ组进一步抑制肿瘤生长速率。相反,荷瘤小鼠的Kaplan-Meier生存曲线显示显著延长的存活率。因此,为了了解联合治疗的毒性作用,研究人员同时监测了体重变化。结果表明,两组之间的体重变化无显著差异。此外,免疫组织化学染色显示,TMZ-US增加了肿瘤组织中的DNA损伤(γ-H2AX)和凋亡(裂解的caspase3),并降低了与细胞增殖和侵袭相关的多种指标的表达,包括Ki67、MMP2和N-Cadherin,这些结果表明,TMZ-US疗法增强了DNA的TMZ损伤,诱导了更高的凋亡和更低的侵袭性(图2)。

图2 TMZ+US联合比TMZ治疗能更好地抑制肿瘤生长
3. 差异甲基化基因和差异表达基因的综合分析
作者使用多组学分析来探讨TMZ-US对胶质瘤细胞产生的影响。转录组学分析TMZ-US诱发的肿瘤死亡机制。首先,对比NC、TMZ和TMZ-US,结果识别出5005个差异。KEGG对这些差异表达基因的富集分析显示,TNF信号通路与TMZ-US效应关系最为密切。接下来,为了进一步研究TMZ-US疗法的机制,进行了多组学分析。基于RNA-seq的KEGG结果,分析了肿瘤坏死因子(TNF)的启动子甲基化。结果表明,与TMZ组相比,该启动子发生了超甲基化。最后,对TMZ-US和TMZ-US的DEGs进行了综合分析。综合多组学分析和实验结果,可以发现TMZ-US引起TNF-α表达水平升高,这可能与其启动子甲基化水平降低有关。此外,也发现坏死凋亡得到富集(图3)。
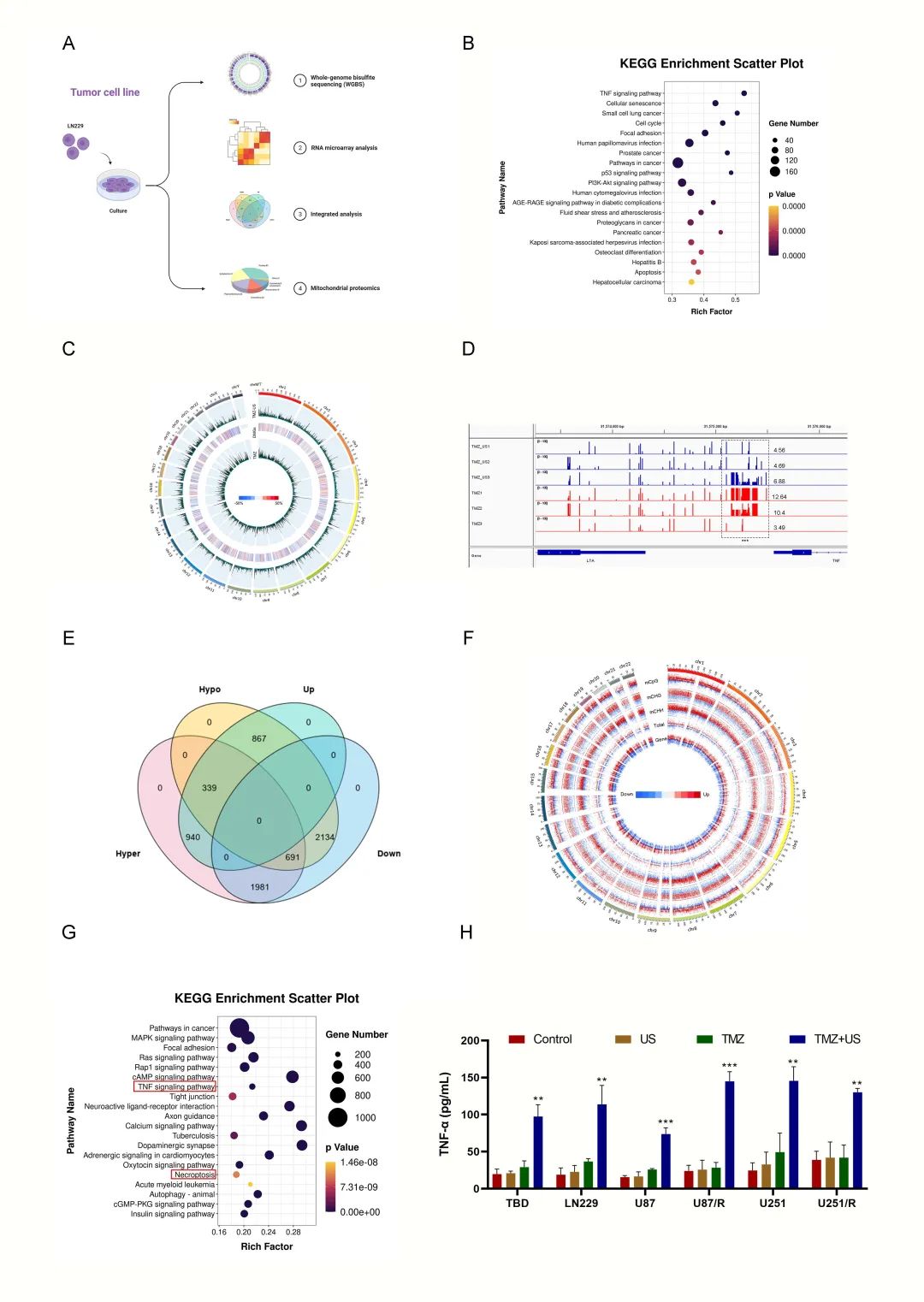
图3 WGBS与RNA-seq的综合分析
4. TMZ-US通过增加ROS诱导胶质瘤细胞的坏死凋亡
根据综合分析结果,探查了细胞坏死性凋亡,以确定原发性细胞损伤是否由TMZ-US引起。首先,我们使用了各种细胞死亡抑制剂来探查TMZ-US治疗后的细胞死亡模式。发现在较高的TMZ浓度下,细胞出现坏死性下垂。进一步探索了联合治疗后不同抑制剂浓度对细胞的作用,Nec-1和NAC对TMZ-US诱发的细胞死亡具有剂量依赖性效应。ROS水平升高导致TMZ-US诱导的坏死凋亡。进行Western blotting分析结果显示,TMZ-US上调了p-RIP1、p-RIP3、p-MLKL或RIP1、RIP3、MLKL,但NAC阻止了这种上调。此外,在ATP浓度测定中也获得了类似的结果。这些结果均表明TMZ-US激活ROS诱导细胞坏死凋亡(图4)。
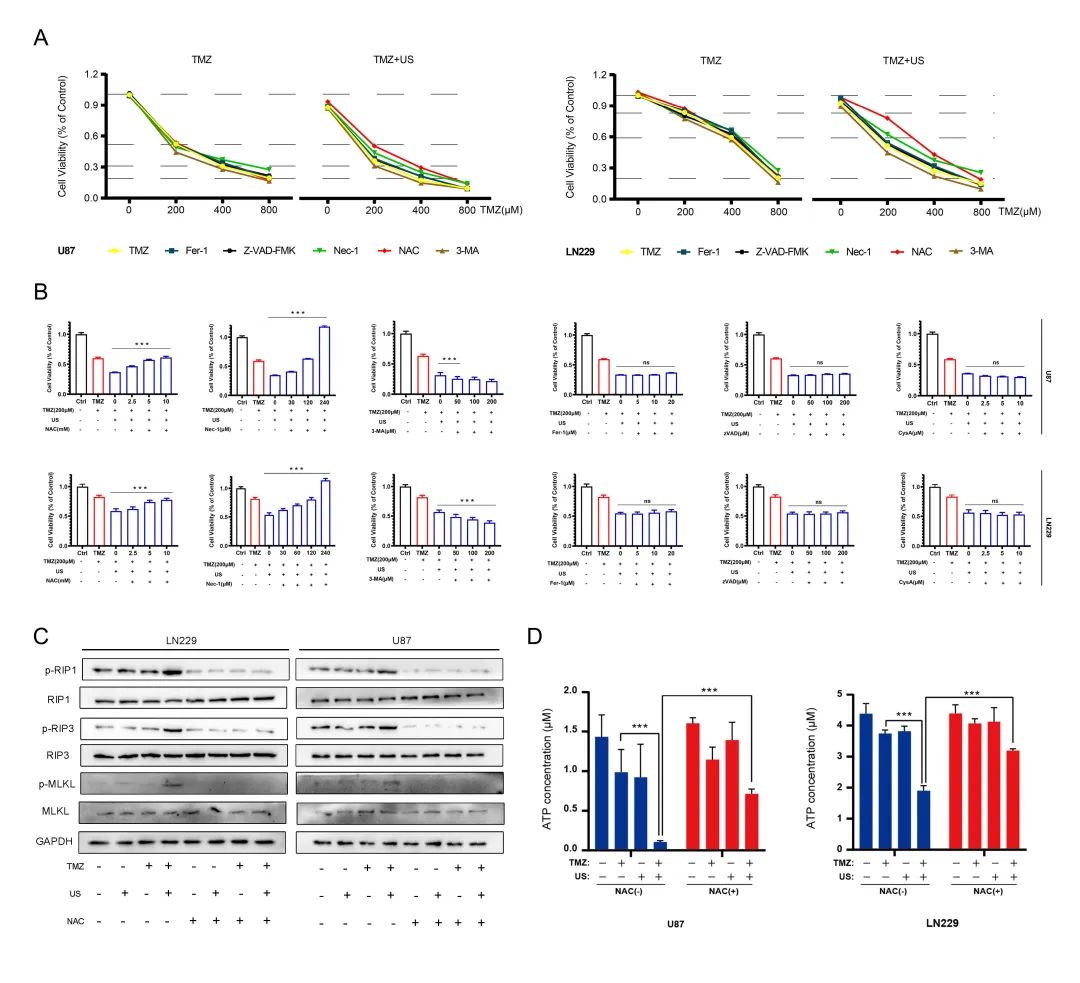
图4 TMZ + US通过增加活性氧诱导胶质瘤细胞坏死
5. TMZ-US不能诱导线粒体依赖性细胞凋亡
为进一步探索TMZ-US对线粒体依赖性凋亡的影响。研究人员对细胞色素c与线粒体共定位和线粒体蛋白质组学研究。得出以下结论: 1、TMZ-US主要影响细胞核内的位点;2、TMZ-US不影响与线粒体依赖性凋亡有关的蛋白;3、TMZ-US主要影响生物过程(图5)。
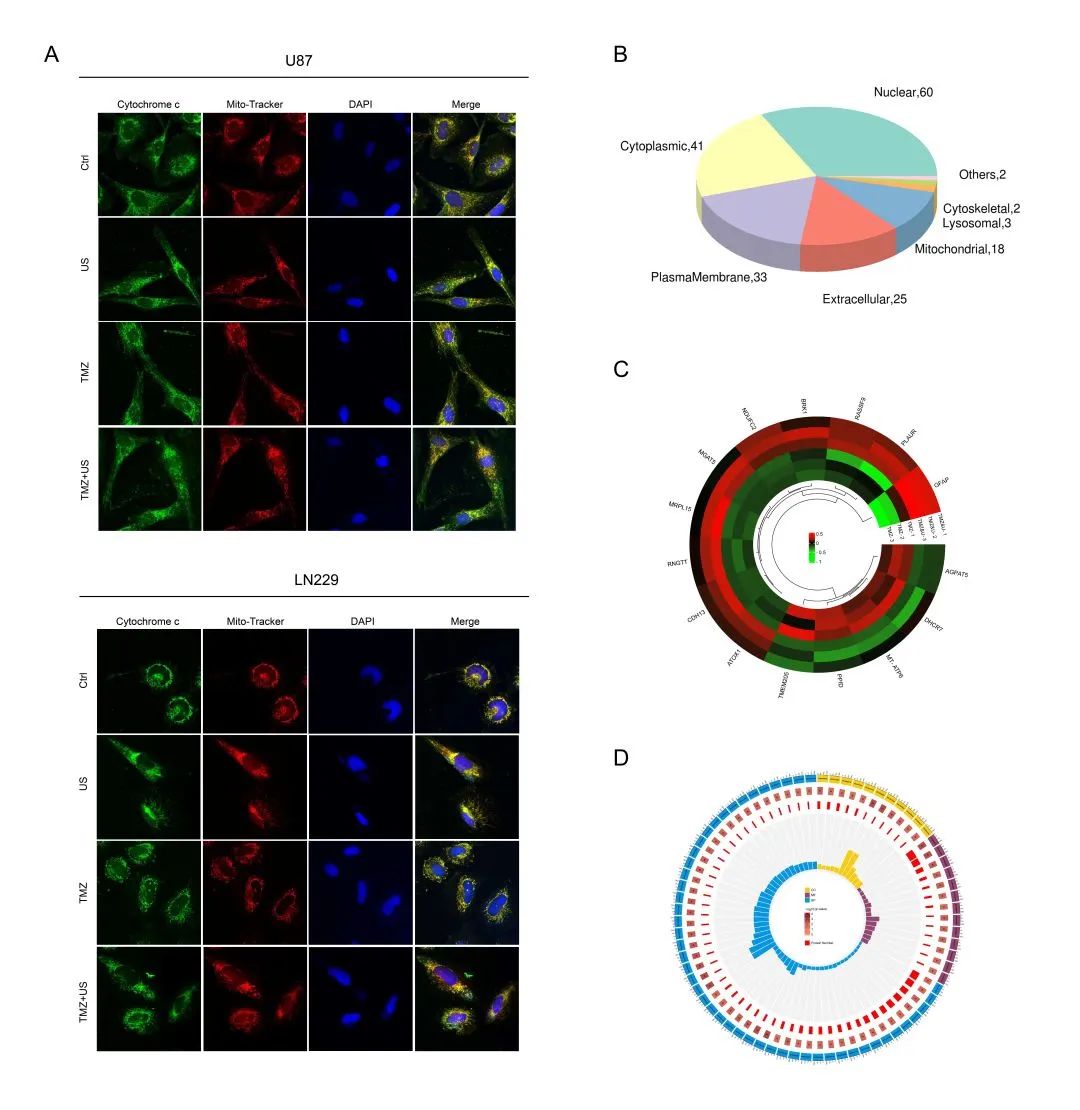
图5 TMZ-US不能诱导线粒体依赖性细胞凋亡
文章小结
本研究提出了TMZ对GBM的超声动力化疗。本文通过理论计算和实验证实TMZ可能是一种超声作用下产生ROS的声敏剂。此外,TMZ-US在体内和体外均可增强TMZ化疗疗效,逆转TMZ耐药。最终,通过多组学综合分析并实验验证,TMZ-US主要通过ROS诱导胶质瘤细胞的坏死凋亡发挥抗肿瘤作用。本文工作主要在天津市环湖医院神经外科研究所完成。文章的第一作者分别是王钒臣(天津医科大学研究生)、徐立霞、闻斌礼(天津医科大学研究生);通讯作者是闫华、佟小光、王银松(天津医科大学)。
中科优品推荐
【中科新生命】经过19年的时间积累,现已建立起了Labelfree、TMT、4D-Labelfree、4D-DIA、4D-labelfree修饰、DIA磷酸化、外泌体多组学等多种蛋白组学平台以及代谢、转录平台。此外,中科新生命有着专业的数据分析平台以及售前售后服务团队,为老师提供全面的技术支持。欢迎感兴趣的老师前来咨询。

